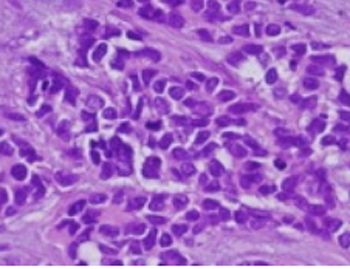
Histológicamente el tumor desmoplásico de células pequeñas y redondas, se caracteriza por la presencia de nidos de células malignas pequeñas que se encuentran dentro de un estroma fibroso denso. En el diagnóstico diferencial se debe incluir el sarcoma de Swing, rabdomiosarcoma, nefroblastoma, neuroblastoma, mesotelioma, tumor radoide, adenocarcinoma metastático o avanzado.
Su principal característica diagnostica viene marcado por 2 puntos fundamentales: 1. Perfil inmunohistoquímico. Positividad de los marcadores polifenotípicos con una coexpresión epitelial (keratina, antígeno de membrana epitelial), mesenquimal muscular (desmina y vimentina) y, neural (neuroenolasa específica) 5. 2. Citogenética. Translocación t(11;22) (p13;q12), la cual implica la fusión de los genes EWS y WT1 5,6.
A pesar de los tratamientos agresivos con resección quirúrgica, quimioterapia a altas dosis, transplante de células madre y radioterapia, la recidiva o la progresión de este tipo de tumores es la regla, describiéndose una supervivencia media menor de 2 años 6,7. En nuestro caso la re-resección y los nuevos ciclos de quimioterapia se plantean como una posibilidad, para prolongar la sobrevida media.
Actualmente existen varios ensayos clínicos en fase II, utilizando terapia molecular dirigida con mesilato de imatinib, que ha demostrado su eficacia en: leucemia mieloide crónica y, en GIST metastáticos; bloqueando los receptores tirosinkinasa e impidiendo así, la replicación descontrolada de las células 8. Y otros estudios (AMG 479), también en fase II, utilizan anticuerpos monoclonales (IgG1), frente a receptores de factores de crecimiento similares a la insulina (IGF-1R), y que parecen conseguir una inhibición en el crecimiento de las células tumorales 9.
En niños se han comenzado a usar terapias similares a la que se utilizan en las carcinomatosis peritoneales en pacientes adultos, como es la perfusión peritoneal hipertérmica continua 10 y el trasplante autólogo de células madre de médula ósea 11.
En general podemos decir que se necesitan equipos multidisciplinares y probablemente centros especializados en la revisión oncológica e histológica de estos pacientes, o al menos intentar aumentar el número de pacientes incluidos en los ensayos clínicos, para que las conclusiones obtenidas sean más fiables 12.
FIGURAS
Figura 1. Radiografía de abdomen. Dilatación de asas de intestino delgado.
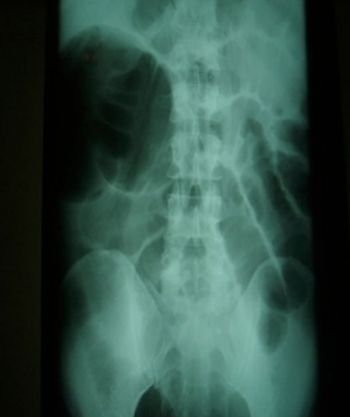
Figura 2. Tomografía axial computada que muestra imagen de obstrucción intestinal.
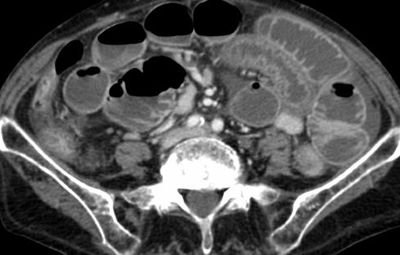
Figura 3. Imagen de pieza quirúrgica.
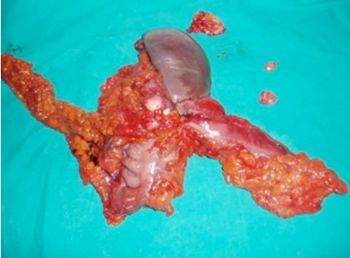
Figura 4. Anatomía patológica, tumor desmoplásico.
BIBLIOGRAFÍA
- Gerald WL, Rosai J. Desmoplastic small cell tumor with divergent differentiation. Pediatr Pathol 1989;9(2):177-83.
- Jellouli M, Mekki M, Krichene I, Zakhama A, Belghith M, Jouini R, et al. Intra-abdominal desmoplastic small round cell tumor in childhood: case report and review of the literature. Bull Cancer. 2003;90(12):1063-6.
- Adsay V, Cheng J, Athanasian E, Gerald W, Rosai J. Primary Desmoplastic Small Cell Tumor of Soft Tissues and Bone of the Hand. Am J Surg Pathol. 1999;23(11):1408-13.
- C. E. Stuart-Buttle CE, C. J. Smart CJ, S. Pritchard S, D. Martin D, and I. M. Welch IM, Desmoplastic small round cell tumour: a review of literature and treatment options. Surgical Oncology. 2008;17(2):107–112, 2008.
- Chang F. Desmoplastic small round cell tumors: cytologic, histologic, and immunohistochemical features. Arch Pathol Lab Med. 2006;130:728-32.
- Rekhi B, Ahmed S, Basak R, Qureshi SS, Desai SS, Ramadwar M, Desai SB, Kurkure P, Jambhekar NA. Desmoplastic small round cell tumor-clinicopathological spectrum, including unusual features and immunohistochemical analysis of 45 tumors diagnosed at a tertiary cancer referral centre, with molecular results t(11; 22) (p13; q12) (EWS-WT1) in select cases.Pathol Oncol Res. 2012;18(4):917-27.
- Presley AE, Kong CS, Rowe DM, Atkins KA. Cytology of desmoplastic small round-cell tumor: comparison of pre- and post-chemotherapy fine-needle aspiration biopsies. Cancer. 2007;111:41-6.
- Mearadji A, den Bakker MA, van Geel AN, Eggermont AM, Sleijfer S, Verweij J, et al. Decrease of CD117 expression as possible prognostic marker for recurrence in the resected specimen after imatinib treatment in patients with initially unresectable gastrointestinal stromal tumors: a clinicopathological analysis. Anticancer Drugs. 2008;19:607-12.
- Naing A, LoRusso P, Fu S, Hong DS, Anderson P, Benjamin RS, et al. Insulin growth factor-receptor (IGF-1R) antibody cixutumumab combined with the mTOR inhibitor temsirolimus in patient with refractory Ewing’s sarcoma family tumors. Clin Cancer Res. 2012;18:2625-31.
- Hayes-Jordan A1, Green HL, Lin H, Owusu-Agyemang P, Fitzgerald N, Arunkumar R, Mejia R, Okhuysen-Cawley R, Mauricio R, Fournier K, Ludwig J, Anderson Complete cytoreduction and HIPEC improves survival in desmoplastic small round cell tumor. Ann Surg Oncol. 2014;21(1):220-24.
- Bisogno G, Ferrari A, Rosolen A, Scarzello G, Garaventa A, Arcamone G, Carli M: Sequential intensified chemotherapy with stem cell rescue for children and adolescents with desmoplastic small round-cell tumor. Bone Marrow Transplant 2010, 45(5):907-11.
- Lettieri CK, Garcia-Filion P, Hingorani P. Incidence and outcomes of desmoplastic small round cell tumor: results from the surveillance, epidemiology, and end results database. J Cancer Epidemiol. 2014; 680126.